KEVIN ALEXANDER CALIMEÑO SECAIDA
el tema que nos toco fue el ENLACE QUIMICO
 Estos son 2 de los 5 alumnos que asistieron a la reunion que se hizo en mi casa el dia 20 de julio a las 2 de la tarde
Estos son 2 de los 5 alumnos que asistieron a la reunion que se hizo en mi casa el dia 20 de julio a las 2 de la tardesus nombres izquierda a derecha:
LUIS FELIPE BORJA LEON
HARRY JEFFERSON ROMAÑA.
 Este es otro alumno que asistio el mismo dia su nombre es
Este es otro alumno que asistio el mismo dia su nombre es LUIS FERNANDO PALACIOS PALACIOS.
LUIS CARLOS LOPEZ MARTINEZ.
KEVIN ALEXANDER CALIMEÑO SECAIDA
 Aqui nos encontramos todos luego de reunir todo lo propuesto a buscar por ejemplo
Aqui nos encontramos todos luego de reunir todo lo propuesto a buscar por ejemplo
 Aqui nos encontramos todos luego de reunir todo lo propuesto a buscar por ejemplo
Aqui nos encontramos todos luego de reunir todo lo propuesto a buscar por ejemplo LUIS FELIPE, HARRY JEFFERSON Y LUIS FERNANDO
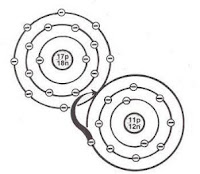
ENCONTRARON ESTAS IMAGENES:
LUIS CARLOS Y YO ( KEVIN ALEXANDER CALIMEÑO SECAIDA )
encontramos el concepto de este:
encontramos el concepto de este:
ENLACE QUIMICO
Un enlace químico es el proceso físico responsable de las interacciones atractivas entre átomos y moléculas, y que confiere estabilidad a los compuestos químicos diatómicos y poliatómicos. La explicación de tales fuerzas atractivas es un área compleja que está descrita por las leyes de la electrodinámica cuántica.[] Sin embargo, en la práctica los químicos suelen apoyarse en la mecánica cuántica o en descripciones cualitativas que son menos rigurosas, pero más sencillas en su descripción del enlace químico. En general, el enlace químico fuerte está asociado con la compartición o transferencia de electrones entre los átomos participantes. Las moléculas, cristales, y gases diatómicos -o sea la mayor parte del ambiente físico que nos rodea- está unido por enlaces químicos, que determinan la estructura de la materia.
Los enlaces varían ampliamente en su fuerza. Generalmente, el enlace covalente y el enlace iónico suelen ser descritos como "fuertes", mientras que el enlace de hidrógeno y las fuerzas de Van der Waals son consideradas como "débiles". Debe tenerse cuidado porque los enlaces "débiles" más fuertes pueden ser más fuertes que los enlaces "fuertes" más débiles.
Los enlaces varían ampliamente en su fuerza. Generalmente, el enlace covalente y el enlace iónico suelen ser descritos como "fuertes", mientras que el enlace de hidrógeno y las fuerzas de Van der Waals son consideradas como "débiles". Debe tenerse cuidado porque los enlaces "débiles" más fuertes pueden ser más fuertes que los enlaces "fuertes" más débiles.
Nos propusimos a buscar videos, y encontrar un poco mas de este tema tan interesante.
Hubo un alumno que no asistio por encontrarse enfermo:
HARRY BELTRAN CASTAÑO












No hay comentarios:
Publicar un comentario